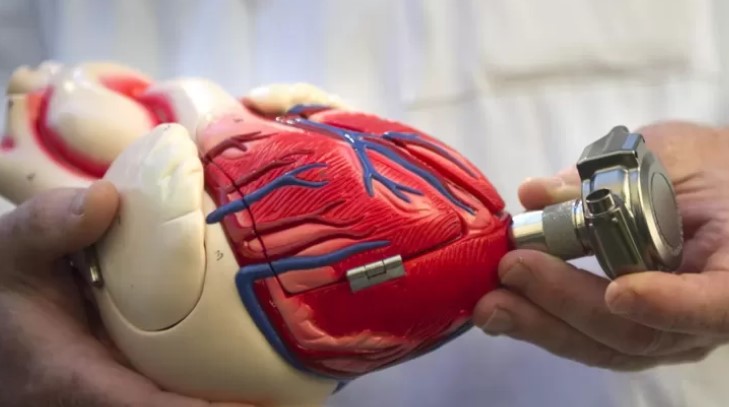
Вместо того, чтобы заменить сердце, хирурги разработали механические устройства, чтобы помочь ему перекачивать кровь. От поездки человека в луну до генотического инженера и искусственного интеллекта. Научные достижения человечества XXI века выходят за рамки возможных. Так почему же создание искусственного сердца была такой сложной задачей?
Ничто так не так хорошо доказывает совершенство человеческого сердца, как неудачные попытки имитировать его. И история искусственного сердца сопровождается как блестящими инновациями, так и постоянными неудачами.
В 1961 году президент США Джон Кеннеди провозгласил амбициозную цель Соединенных Штатов — к концу десятилетия космический полет с приземлением космонавтов на поверхности Луны.
А в 1964 году сердечно -сосудистый хирург Майкл Дебейки убедил президента США Линдона Б. Джонсона финансировать развитие первого искусственного сердца.
В 1969 году обе цели, казалось, были достигнуты. Миссия Аполлона-11 была успешной, и человек сделал первые шаги на Луне.
В то же время Техасский институт сердца имплантировал первое полностью искусственное сердце. Но после трансплантации у пациента были осложнения, и он умер в тот же день.
Первоначально врачи думали, что искусственное сердце навсегда заменит больные. Тем не менее, цель была слишком амбициозной, потому что в первой структуре был внешний компрессор, который был введен через кожу в тело пациента.
С одной стороны, это было полезно, потому что механические детали (наиболее подверженные износу) можно было легко заменить, но пациенту пришлось носить громоздкое оборудование.
История искусственного сердца также тесно связана с историей его трансплантации. В начале 1960 -х это была лишь обнадеживающая мечта, но в 1967 году хирург сердца Кристиан Барнард из Кейптауна провел первую успешную пересадку человеку в мире.
Назначение первых искусственных сердец также изменилось. Теперь они должны были поддерживать кровообращение, в то время как пациент ожидает донорское сердце.
Как и во многих экспериментальных методах лечения, первым при хирурге был пациент на терминальной стадии.
Он стал 47-летним Хаскеллом Карпом. Человек страдал от острой сердечной недостаточности и пережил несколько сердечных приступов. Состояние ухудшилось, и не было соответствующего тела доноров. Затем они решили временно пересадить искусственное сердце до появления соответствующего человека.
Операция длилась 3 часа, с 16 врачами. Все было успешным, и сердце работало в течение трех дней — до тех пор, пока донорский орган не был найден.
Сначала это казалось триумфом, но в течение 32 часов пациент трагически умер от сепсиса. Более того, устройство повредило кровь и почки.
Инфекции и сепсис являются постоянной проблемой для любого устройства, где есть провода, которые используют кожу.
И это еще не все.
Насосы, которые качают кровь, изменяют его состав, вызывают свертывание крови, что приводит к инсультам и расщеплению эритроцитов.
Но наука не стояла на месте, и через десять лет хирург сердца Роберт Джарвик создал искусственное сердце улучшенной структуры, которое было дано его имени.
В 1982 году первым получателем этого протеза был стоматолог Барни Кларк, который жил с ним почти три с половиной месяца.
В течение следующих трех лет протез Jarvik-7 был поглощен еще пятью безнадежными пациентами, один из которых он дал более двадцати месяцев своей жизни.
Но у двух других пациентов были тяжелые удары, и в конечном итоге они умерли от сепсиса или проблем с крови.
Разработка кардио -трансплантации также была нелегкой: первый пациент умер в течение 18 дней после операции. Первый пациент в Британии жил всего 45 дней, и общие показатели оставались разочаровывающими.
Тем не менее, причиной отказа была не в механике. Тело было воспринято пересаженным органом как угрозу и начал бороться с ним.
Чтобы избежать этого, пациенту вводили лекарства, которые подавляют иммунную систему.
Первые иммунодепрессанты были простыми, но развитие циклоспорина в начале 1980 -х годов революционизировала иммуносупрессию, что значительно улучшило успех пересадки органов.
Сегодня в Британии производится около 200 пересадков. Тем не менее, хроническая сердечная недостаточность остается одной из самых больших проблем во многих странах мира, и поворот пересадки сердца может быть отложен в течение многих лет.
Чтобы решить эту проблему, ученые начали искать альтернативные способы. Одним из них была беспрецедентная модификация генома свиньи. Ученые ближе к человеку, которые в будущем могут помочь преодолеть отсутствие органов для трансплантации.
Свиньи лучше других животных, потому что их ДНК относительно близко к человеку, внутренние органы одинаковы по размеру. Кроме того, свиней легко разводить в больших количествах.
Первые клинические испытания начались в 2022 году.
Транспанс -успех
Однако меры сердца возродили поиск полного искусственного сердца с более достижимой целью — поддерживать жизнь пациента, пока они не найдут донора.
В течение десятилетий искусственные технологии сердца были улучшены благодаря более биосовместимым материалам, улучшению конструкции клапана и более эффективным контролем крови.
Поскольку поворот пересадки сердца может быть отложен в течение многих лет, пациент часто подключается к устройству вспомогательного анализа SO -называемого VAD (вспомогательное желудочковое устройство). Полимеханический имплантат только облегчает работу больного сердца, но не заменяет его. Он был создан как временное средство жизни, а не как основной метод терапии.
Однако, поскольку он все чаще используется VAD, особенно в течение длительного времени (в течение периода даже четырех лет), врачи все чаще начинают обращать внимание на преимущества такого насоса по сравнению с другими формами кардиотерапии и, прежде всего, лекарства.
Следующим революционным шагом была разработка вспомогательного устройства для левого желудочка сердца (LVAD).
Это имплантированный механический насос, который поддерживает сердце у людей со слабыми сердечными мышцами. Он берет кровь из нижней камеры сердца и помогает перекачивать ее в другие жизненно важные органы.
LVAD стал спасательным кругом в лечении сердечной недостаточности на терминальной стадии.
Сегодня в мире было имплантировано более 15 000 LVAD, около трети пациентов с терминальной сердечной недостаточностью поддерживаются этим устройством. Обычно LVAD используется временно, поскольку пациент ожидает донорского сердца, но из -за дефицита донорских органов пациенты могут оставаться в поддержке LVAD в течение многих лет.
Однако все упомянутые устройства имеют недостатки. Обычно они состоят из двух частей — имплантированных, соединенных непосредственно к сердцу и соединены с ним проводами внешней системы, содержащей контроллер и источник питания.
Внешние батареи по -прежнему вызывают неудобства и являются источником инфекции для пациентов.
Следовательно, поиск искусственного сердца, которое полностью имплантируется, активен.
Никто не ожидает, что это будет быстро и легко. И многочисленные многолетние неудачи, конечно же, вызвали смирение и почтение к естественной инженерии сердца.